2019年5月28号,我院靳津实验室在Journal of Clinical Investigation(JCI)发表题为“USP16-mediated deubiquitination of calcineurin A controls peripheral T cell maintenance”的研究论文,揭示了USP16调控成熟T细胞的活化的关键作用与机制,并发现USP16可作为T细胞介导的自身免疫病的潜在治疗靶点。
USP16为一种去泛素化酶,既往研究发现其在有丝分裂的染色体分离过程中发挥重要作用,同时其异常表达与唐氏综合征相关。除了多脏器发育障碍外,唐氏综合征病人常伴有急性淋巴细胞白血病和乳糜泻的发病,但其免疫系统异常活化的机制尚不明确,USP16在这类免疫性疾病中的功能也缺少研究。该文从患有不同自身免疫性疾病的患者体内分离的外周CD4+ T细胞均表现出 USP16 升高,但USP16 诱发T细胞过度活化的具体机制仍不明了。
本文发现,在T细胞中条件性敲除USP16的小鼠对多种自身免疫性疾病的易感性降低。在感染实验性自身免疫性脑脊髓炎(EAE)中,T细胞特异性敲除USP16小鼠的临床症状比野生型更轻微、脑及脊髓中炎症细胞的浸润也较少;在T细胞过继转移诱导的肠炎模型中,T细胞特异性敲除USP16小鼠的致死率显著降低、肠道结构改变减轻,说明USP16参与T细胞介导的自身免疫病的发展。
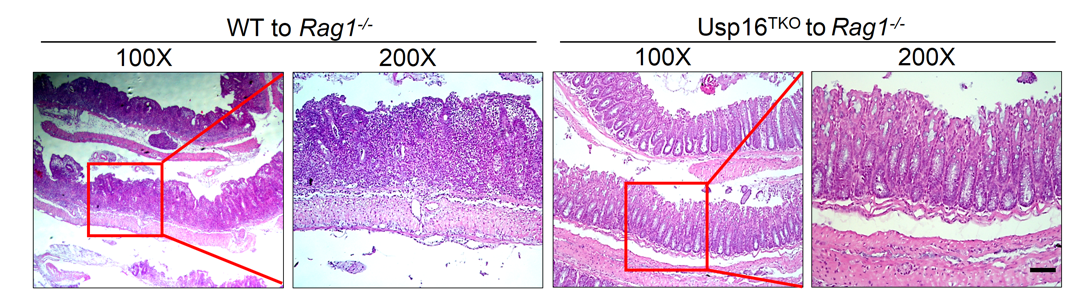
肠炎模型小鼠肠道组织HE染色
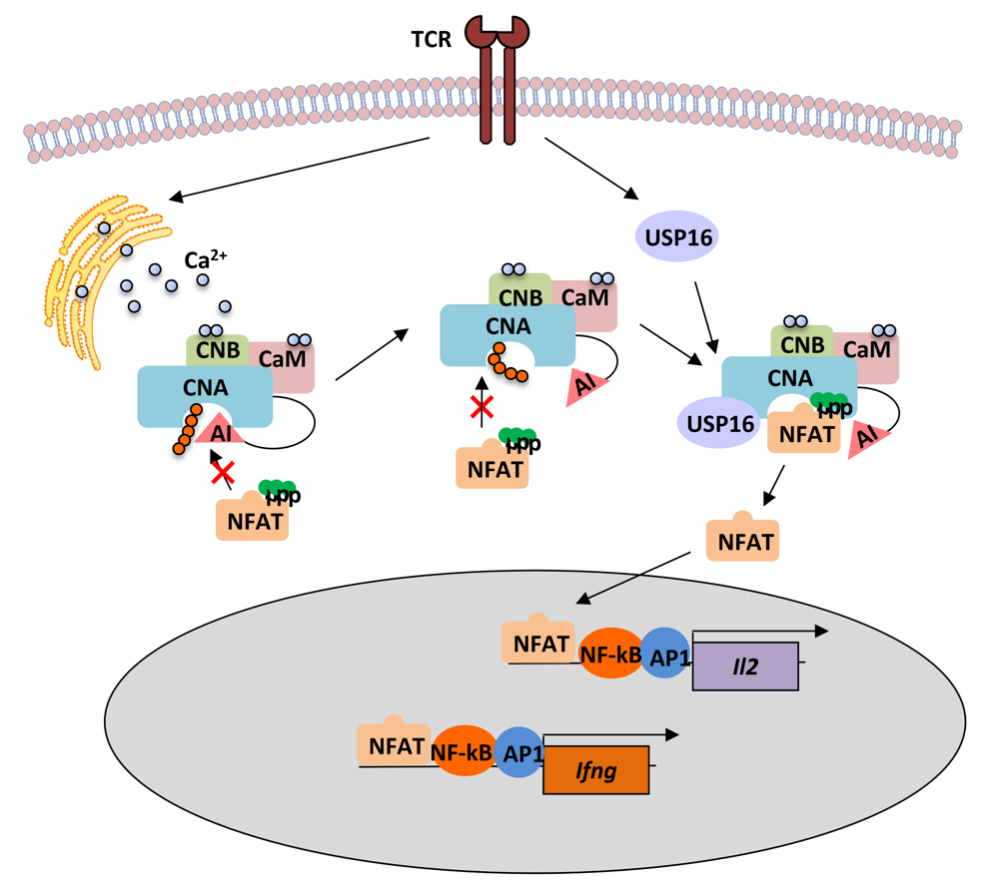
机制研究发现,USP16的缺失使得外周T细胞稳态发生改变,成熟T细胞的活化与增殖也受到影响。进一步生化实验表明,USP16参与TCR启动的Calcineurin-NFAT轴信号通路,其选择性地与Ppp3cb和Ppp3cc编码的CNA结合后,特异性擦除K29-linked多聚泛素化链。而CNA的去泛素化使得下游NFAT活化,向细胞核内转运加强,从而实现对T细胞功能的影响。
该工作首次阐明了USP16通过调节calcineurin-NFATs轴活化对外周T细胞的稳态、活化、增殖的关键作用与机制,并提示USP16可作为T细胞介导的自身免疫性疾病的新型干预靶点。
博士研究生张瑜、刘蓉蓓、范柯琪和浙江大学医学院附属邵逸夫医院曹倩教授为共同一作,靳津教授为本文的通讯作者。该课题得到了国家基金委优秀青年基金、国家基金委面上项目、中组部人才项目、浙江省杰出青年基金的资助。
原文链接:https://www.jci.org/articles/view/123801