组蛋白修饰作为表观遗传信息的主要载体之一,具有调节细胞内基因表达的功能。其中研究较多的H3K36位点甲基化通常被认为是富集于基因间区和基因区的活性标记,其功能包括参与细胞活动,DNA损伤,转录起始,RNA剪切,RNA m6A修饰等。
在此前研究报道中,传统ChIP-seq方法发现H3K36me3主要在活跃基因的gene body区富集,并且从基因的5’端向3’端逐渐增加。H3K36me3的甲基转移酶最初在酵母中鉴定为Set2[1],在哺乳动物细胞中发现其同源蛋白SETD2是H3K36me3的甲基转移酶。此外,精子减数分裂特异性组蛋白甲基转移酶PRDM9被报道在睾丸中同时催化H3K4me3和H3K36me3[2]。
2022年6月9日,我院方东实验室在Nature Communications杂志发表题为“SMYD5 catalyzes histone H3 lysine 36 trimethylation at promoters”的研究论文,发现哺乳动物细胞中,除SETD2外,SMYD5可作为H3K36me3的甲基转移酶,在基因启动子区催化H3K36me3(图1)。
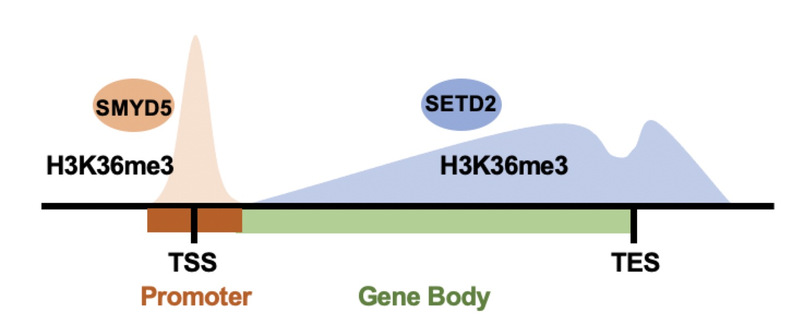
图1. SMYD5催化启动子区H3K36me3,SETD2催化基因区H3K36me3
TSS, transcription start site. TES, transcription end site.
本研究通过CUT&Tag的方法分析了H3K36me3在未交联细胞中的分布情况,此方法利用Tn5转座子剪切并标记DNA,可使细胞内染色体尽可能在自然状态下被标记。通过该方法,课题组首次发现H3K36me3在基因启动子的富集,并且课题组也通过非交联和超声的Native ChIP-seq进行了验证。通过对多种候选蛋白的大规模敲除筛选实验,鉴定得到SMYD5蛋白是潜在的H3K36me3的甲基转移酶,并且在体内体外实验中进行了验证。调控机制上,SMYD5被RNA聚合酶II招募到染色质中,在启动子区域催化H3K36三甲基化修饰,并且其C端富含谷氨酸的结构域调控了SMYD5与组蛋白H3的结合以及对H3K36me3的催化活性。
此外,该研究还发现Smyd5在肝癌细胞中高表达,在小鼠肝癌模型中敲降Smyd5基因能有效抑制肝癌的发生,并且野生型Smyd5的重新表达能够恢复小鼠肝癌形成,C端富含谷氨酸的结构域敲除的Smyd5则不能恢复。该研究为进一步探究H3K36me3的功能以及H3K36me3异常的癌症研究提供了新的思路。
方东研究员为本文通讯作者,浙江大学生命科学研究院博士研究生张燕君、房圆、唐寅为共同第一作者。该研究得到了浙江大学生命科学研究院赵斌教授在小鼠肝癌模型构建上的大力支持,受到国家自然科学基金的资助。
参考文献:
[1] Strahl, B.D. et al. Set2 is a nucleosomal histone H3-selective methyltransferase that mediates transcriptional repression. Mol Cell Biol 22, 1298-1306 (2002).
[2] Powers, N.R. et al. The Meiotic Recombination Activator PRDM9 Trimethylates Both H3K36 and H3K4 at Recombination Hotspots In Vivo. PLoS Genet 12, e1006146 (2016).
原文链接:https://www.nature.com/articles/s41467-022-30940-1