男女有别,雌雄异体是我们司空见惯的自然现象。然而其实绝大多数的植物没有性别,或者为雌雄同株。鲜为人知的是,即使是动物中,如果我们不考虑昆虫,也有至少三分之一的动物(例如我们熟悉的蜗牛,蚯蚓,藤壶)为雌雄同体,或者在生长发育的不同阶段同一个个体可以经历雌雄转换(如小丑鱼)。因此生物的生殖方式如何由无性演化成有性,以及决定生物性别的性染色体如何起源和演化一直是最为基本和重要的生物学问题之一。但长期以来由于大多数被深入研究的模式物种都为有性生殖物种,距离它们性别或者性染色体最早起源的时间太过久远,这些问题一直没有解答。
2022年6月10日,我院周琦课题组在Nature Communications杂志上发表了题为“Evolution of sexual systems, sex chromosomes and sex-linked gene transcription in flatworms and roundworms”的研究论文,系统阐述了扁形动物门和线虫动物门物种的性别和性别染色体是如何起源和演化的。这两个庞大的分类阶元包含了大量造成人类或者家禽家畜严重疾病的寄生虫。其中包括扁形动物门的血吸虫,其导致的疾病是继疟疾之后世界上传播最广的寄生虫病。世界卫生组织估计直至2022年全球约有7.79亿人面临血吸虫感染风险。而线虫动物门除了科学家熟悉的模式动物秀丽隐杆线虫,也包含了其他会引起疾病的蛔虫,丝虫,鞭虫和钩虫。值得注意的是,许多这些物种在比较晚近的演化时间阶段经历了由无性向有性生殖(或反之)的转换,是不可多得的研究动物性别如何起源的模型。
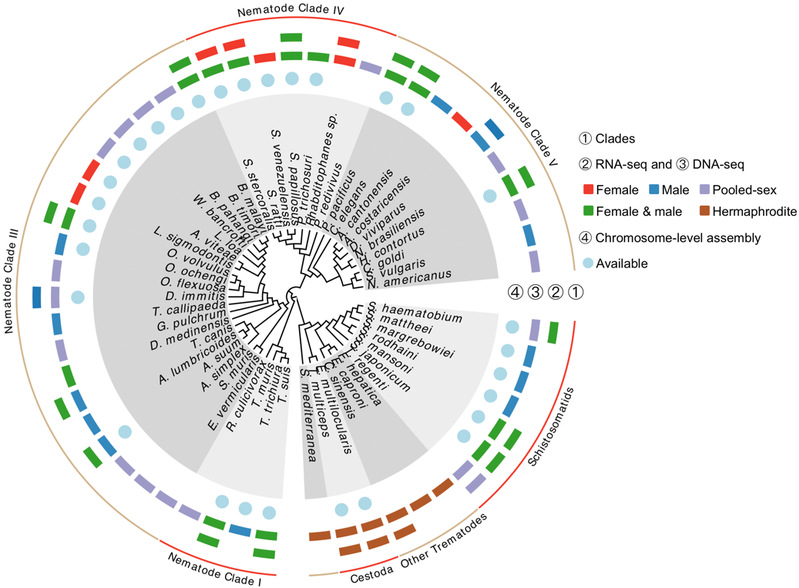
图1 本研究所囊括的物种及其数据类型
作者通过深入挖掘公共数据库中41个线虫门物种和13个扁形动物门物种的基因组和转录组的数据 (图1),首次鉴定出17个线虫门物种的性别相关区域以及它们性别染色体的基本组成。它们的性别染色体是由所有线虫门物种共享的古老的染色体元件(被称为Nigon元件[1],根据著名线虫生物学家Victor Nigon的名字而来;类似果蝇的染色体也根据著名果蝇遗传学家Hermann Muller被命名为Muller元件一样),通过在演化过程中如同不同的乐高积木发生相互不同的组合而成(图2)。 当原本是常染色体的Nigon染色体元件,与古老的性染色体(比如秀丽隐杆线虫的性染色体对应于N和X两个Nigon元件)发生融合或者易位以后,常染色体会逐步演化成为新的性染色体,并且发生重组抑制。像其他古老的性染色体一样,逐步丢失掉不发生重组的性染色体上的基因,直至完全退化甚至完全消失,也就形成了秀丽隐杆线虫或者其他许多线虫物种中的XO性染色体类型(即雌性为XX,雄性没有Y染色体只有一条X染色体)。
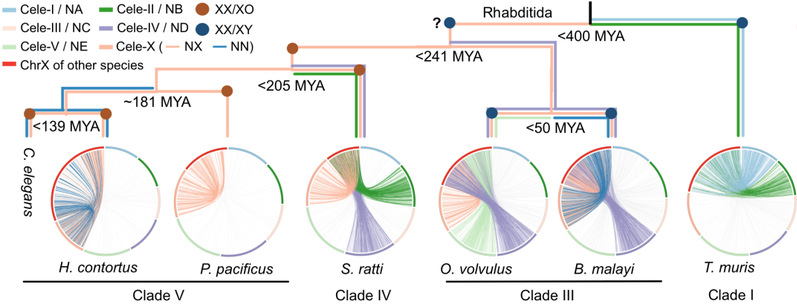
图2 线虫动物门代表物种的性染色体组成
红色圆弧为该物种的性染色体,图中显示了与其同源的其他Nigon染色体单元。不同物种的性染色体由不同的染色体单元组成。
研究进一步发现,这些线虫或者血吸虫在不同的染色体元件相互融合或者易位以后,在演化过程中在不同的时间点发生重组抑制,从而形成了两条性染色体不同区域的“演化断层[2]”。这一模式在周琦课题组前期在哺乳动物和鸟类的性染色体研究中也有报道[3],具体反映为性染色体不同区域之间截然不同的序列分歧度,对应了它们发生重组抑制的不同时间点。
最后,由于扁形动物门中只有吸虫为雌雄异体,其他的物种(如涡虫,绦虫等)都为雌雄同体,而两者分歧仅为70百万年以内[4]。因此通过对它们的比较可以揭示从扁形动物门无性生殖的祖先向有性生殖的吸虫演化过程中,基因组和转录组所发生的变化规律。研究鉴定了一个在果蝇和吸虫中都功能高度保守的雌性相关的基因mag-1,该基因可能发生的隐性突变可能使雌雄同体的祖先雌性不育从而产生雄性个体。其次,第二个突变可能产生了雌性化基因U2AF2[5],从而完成了性别系统的转换过程(图3)。而全基因组水平来说,该转化过程主要涉及性腺转录组偏向去雌性化(即雌雄异体物种卵巢中的基因表达量相比雌雄同体的祖先性腺总体下降)的过程。在线虫动物门中,秀丽隐杆线虫发生了相反的转化,即由雌雄异体的祖先丢失了性别,反向演化为雄性和雌雄同体,而相应地,这一转化主要涉及转录组水平的去雌性化和雄性化。
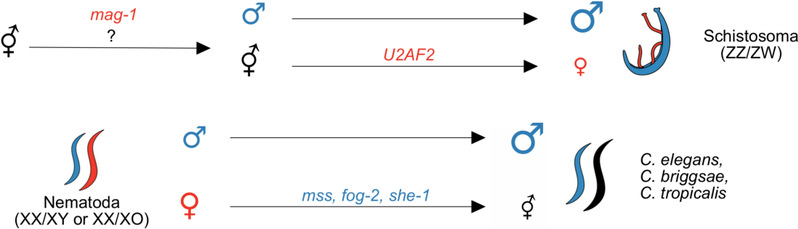
图3 扁形虫和线虫中无性和有性生殖方式相互转换的机制
总结而言,该研究是首次对扁形动物门和线虫动物门物种性染色体演化历史的系统性构建,提供了它们性染色体组成的全面的历史纵览,揭示它们的性染色体的多样性主要是由不同的古老的染色体元件相互融合或易位而造成。而研究中新鉴定的性别连锁的基因,也将对未来通过干扰这些寄生虫的性别繁殖生活史提供重要的依据。本研究是由我院的周琦实验室的博士生王一枫,与澳大利亚墨尔本大学的Robin Gasser教授,和英国爱丁堡大学的Deborah Charlesworth教授共同合作完成。研究受到了国家自然科学基金委面上项目,浙江省自然科学基金,浙江大学生命科学研究院的经费支持。
参考文献:
[1] NIGON V M, FÉLIX M-A. History of research on C. elegans and other free-living nematodes as model organisms [J]. WormBook, 2017, 2017: 1-84.
[2] CHARLESWORTH D. When and how do sex-linked regions become sex chromosomes? [J]. Evolution, 2021, 75(3): 569-81.
[3] ZHOU Q, ZHANG J, BACHTROG D, et al. Complex evolutionary trajectories of sex chromosomes across bird taxa [J]. Science, 2014, 346(6215): 1246338.
[4] OEY H, ZAKRZEWSKI M, NARAIN K, et al. Whole-genome sequence of the oriental lung fluke Paragonimus westermani [J]. Gigascience, 2019, 8(1): giy146.
[5] ELKREWI M, MOLDOVAN M A, PICARD M A, et al. Schistosome W-linked genes inform temporal dynamics of sex chromosome evolution and suggest candidate for sex determination [J]. Mol Biol Evol, 2021, 38(12): 5345-58.
参考网址:
https://news.sciencenet.cn/htmlnews/2018/9/417286.shtm
原文链接:https://www.nature.com/articles/s41467-022-30578-z