近日,我院祝赛勇实验室与浙江大学附属儿童医院傅君芬实验室合作在Cell Reports上发表题为“Single-cell multi-omic analyses highlight the essential role of NKX2.2-CLEC16A/endosomal pathway for human pancreatic differentiation and function”的研究论文,利用实验室近期自主构建的可扩增胰岛前体细胞分化胰岛体系(ePP-islet),系统揭示了干细胞向胰岛分化过程中转录与染色质开放动态变化,并鉴定出NKX2.2-CLEC16A/内体通路这一调控轴在胰岛分化中的关键作用。进一步研究发现CLEC16A敲除模型呈现高免疫原性等特征,为I型糖尿病模型构建提供了新策略;同时,基于ePP-islet系统开展的药物筛选鉴定出IKK抑制剂可有效恢复CLEC16A缺失表型,为后续转化研究提供了重要思路(图1)。
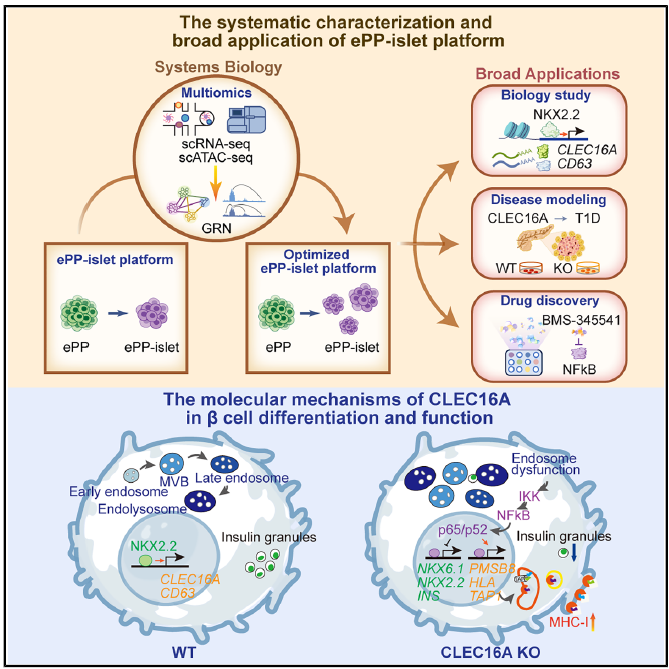
图1. ePP-islet可用于系统性生物学研究,并具有广阔的应用前景
本研究的亮点包括以下几点:
I 破解了胰岛分化的“基因密码”
首先,利用最新的单细胞多组学技术并结合深入的生物信息学分析,系统描绘了ePP向胰岛分化全过程的转录与染色质开放动态景观。这一研究不仅鉴定出调控ePP自我更新、内分泌细胞命运决定及胰岛功能的关键转录因子,还构建了精细的基因表达调控网络,并发现ID家族转录因子在维持ePP细胞自我更新能力以及后续分化过程。
II 揭示了NKX2.2-CLEC16A/内体通路这一调控轴的关键作用
通过整合分析与靶向筛选,首次阐明了NKX2.2与内体通路之间的重要调控关系,证实NKX2.2可直接调控多个内体相关基因;敲低这些基因会严重损害胰岛细胞的生成。此外,NKX2.2在调控胰岛中α细胞、β细胞和δ细胞比例方面亦发挥关键作用。上述发现为理解胰腺发育机制和糖尿病的发生发展提供了新视角。
III 构建了人类特异性I型糖尿病全新研究模型
进一步研究发现,CLEC16A敲除的胰岛细胞不仅分化受阻、功能受损,还出现内体系统紊乱,并显著激活炎症及MHC-I相关免疫通路,其分子特征与自身免疫性I型糖尿病患者β细胞高度相似。尤为重要的是,这些关键现象此前从未在小鼠相关模型中被观察到,凸显了人类干细胞模型在解析疾病机制中的独特价值,为I型糖尿病研究开辟了新方向。
IV 提供了潜在治疗新策略
随后,研究团队利用ePP-islet体系开展化学小分子筛选,成功鉴定出IKK抑制剂能够显著逆转CLEC16A缺陷引起的分化障碍与功能异常,为开发针对相关基因突变型糖尿病的治疗药物提供了重要线索。
总体而言,该研究系统性地解析了ePP-islet体系的生物学特性与应用价值,证明其不仅可用于深入揭示细胞命运决定的分子机制,还能够精准模拟人类疾病特征,并为I型糖尿病的发病机制研究与药物筛选开辟了新路径。
我院祝赛勇研究员和浙江大学附属儿童医院傅君芬教授为论文的共同通讯作者。博士生陈果、2020届博士毕业生马晓洁和博士生蒋利玲为论文的共同第一作者。浙江大学附属儿童医院吴蔚主任在研究中提供了重要支持。该研究获得浙江省自然科学基金、国家自然科学基金及科技部重点研发计划等项目资助。
原文链接: https://www.cell.com/cell-reports/fulltext/S2211-1247