2026年2月26日,我院陆华松研究员课题组和复旦大学生物医学研究院胡晋川研究员课题组合作在《Nature Structural & Molecular Biology》期刊在线发表题为“Integrator subunit INTS12 links ribotoxic stress to transcription-coupled nucleotide excision repair” 的研究论文。该研究首次揭示了ZAK-INTS12信号轴是连接胞质RNA损伤信号与核内TC-NER的关键桥梁,阐明了其在清除停滞Pol II,促进DNA修复,进而维护基因组完整性方面的核心功能。我院博士研究生李卓、杨敏,以及合作者李然、黄彦超是该论文的共同第一作者,陆华松研究员和胡晋川研究员是本文共同通讯作者。
正常的转录与翻译活动对维持细胞活性与功能至关重要。然而,转录的模板——DNA和翻译的模板——RNA都会受到各种内源与外源因子的攻击,产生的DNA与RNA损伤分别阻碍转录和翻译的正常进行。紫外线是最常见的环境毒性因子,当细胞遭受紫外线照射,基因毒性胁迫随之而来。一方面,紫外线直接在DNA上产生嘧啶二聚体等螺旋扭曲损伤,这些损伤像路障一样阻碍RNA聚合酶II(Pol II)的前向易位,导致转录过程受阻。为此,细胞进化出专门的修复途径——转录偶联核苷酸切除修复(TC-NER),它能快速高效地清除活跃转录区域内的DNA损伤,确保关键基因的完整性。另一方面,紫外线同样会诱导RNA损伤,在胞质中触发核糖体毒性应激反应(Ribotoxic Stress Response, RSR)。这一应答过程由ZAK激酶识别阻滞的核糖体激活,相当于胞质内的警报系统被拉响。长期以来,这两条应激通路被视为平行发生的事件。然后,两者之间是否存在对话?RNA损伤信号能否作为“预警信号”,协调和促进核内的DNA修复过程?这些问题尚未得到解答。
为解析RNA损伤信号如何影响核内DNA修复,研究团队聚焦于一个长期被忽视的转录因子——Integrator复合物的柔性亚基INTS12。研究发现,在紫外线照射下,RNA损伤首先在细胞质中激活了ZAK激酶介导的RSR信号通路。令人惊喜的是,这条细胞质内的警报系统,会通过磷酸化修饰的方式,将信号传递给细胞核内的INTS12。在分子机制层面,研究表明,被RSR通路激活的INTS12,其与DNA修复关键因子CSB的相互作用显著增强。这种增强的亲和力,使得INTS12能够招募Integrator复合物至被损伤阻滞的Pol II上,促进其清除,从而为后续的TC-NER修复机器腾出空间,促进DNA修复。当INTS12介导的这一通路被破坏时,细胞清除受阻Pol II的能力下降,转录无法及时恢复,导致细胞对紫外线损伤的敏感性增加。有趣的是,这一机制展现出了高度的情境依赖性:在面对甲醛等诱导的DNA-蛋白质交联损伤(DPC)时,INTS12并不发挥作用,甚至还会抑制DPC通过蛋白酶体降解途径的修复过程,表明细胞会根据损伤类型的不同,灵活选择不同的“清障”策略。
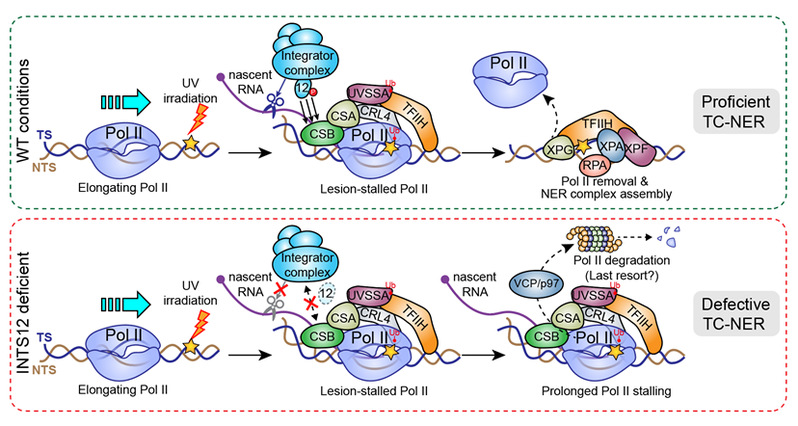
图1:INTS12在TC-NER中的调控功能
综上,该研究系统揭示了一条从RNA损伤到DNA修复启动的完整信号通路。这一机制恰如“矿井中的金丝雀”(Canary in the coal mine)。由于金丝雀对有毒气体高度敏感,旧时煤矿工人常携带其下井,用于指示危险“前兆”。在细胞中,紫外线诱导的RSR,如同最先感知并发出预警的金丝雀,将损伤信号传递至细胞核。随后,INTS12发生磷酸化修饰,进而招募Integrator复合物至停滞的Pol II,促进TC-NER修复过程,从而在基因毒性胁迫下维护基因组完整性(图1)。这些发现深化了我们对RNA损伤信号与DNA修复通路之间耦联机制的理解。
该研究的开展得到了本院焦会朋、方东、杨兵、李磊、黄俊、张龙等老师和共享服务平台的大力支持,研究经费主要来自于国家自然科学基金和浙江省自然科学基金等。陆华松课题组长期聚焦于无膜凝聚体与基因表达在基因组稳定性维持、压力应答、肿瘤发生及细胞衰老等过程中的作用机制研究。目前实验室多个方向的课题正在深入推进,欢迎对相关研究感兴趣的同学联系与加入。
实验室主页:http://lsi.zju.edu.cn/syssy_40763/list.htm
原文链接:https://www.nature.com/articles/s41594-026-01766-y