2026年3月13日,我院林世贤实验室合作在《自然化学》杂志发表了题为“Recoding multiple rare codons enables the simultaneous incorporation of up to five distinct noncanonical amino acids”的研究论文。该研究工作提出使用特定的多种稀有密码子代替空白密码子用于遗传编码非天然氨基酸的新思路,设计并开发了“多重稀有密码子重编码”(Multi-type Rare Codon Recoding)技术。通过对密码子的系统评估和正交翻译系统的适配改造,该技术高效合成了带有两到三种不同类型非天然氨基酸的蛋白质,并在哺乳动物细胞中成功合成了带有多达五种不同非天然氨基酸类型的蛋白质。
几乎所有生物体的遗传密码都是一个由64个三联体密码子组成的通用语言系统,这些密码子被充分用于编码20种天然氨基酸。将这20种天然氨基酸之外的非天然氨基酸进行定点引入,能够极大地提升我们对生物系统的研究与操纵能力。然而,目前的遗传密码拓展技术主要依赖于终止密码子编码,在翻译过程中终止密码子会受到天然翻译释放因子的强烈竞争。这导致大多数非天然氨基酸的编码效率较低,特别是尝试在同一蛋白质中同时引入多种不同类型的非天然氨基酸时,合成效率会呈指数级下降。因此,目前该技术在哺乳动物细胞中的应用绝大多数仍局限于单一类型非天然氨基酸的引入,严重制约了其在更复杂生物学过程研究中的广泛应用。
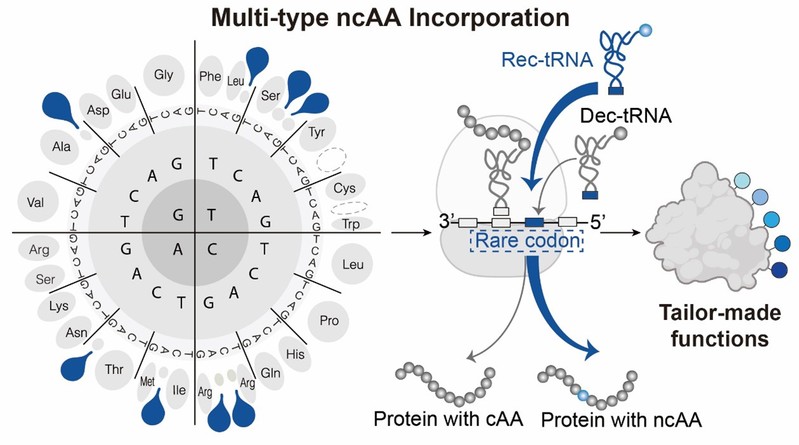
图1. 多重稀有密码子重编码体系的开发和应用示意图
针对这一核心难题,林世贤实验室与合作者创新性地提出了多重稀有密码子重编码策略。实验室对人类基因组中所有稀有密码子的重编码能力和蛋白质组背景引入水平进行了全面评估,成功鉴定出8种能够实现非天然氨基酸高效编码的稀有密码子。研究人员重点利用其中重编码表现最出色的4种稀有密码子(TCG、ACG、CGA和TCA),结合相互正交的氨酰-tRNA合成酶/tRNA对,建立了高效的多重稀有密码子编码体系。该技术不仅广泛兼容目前常用的多种正交翻译系统,还成功应用于双重生物正交标记和蛋白质活性的双重激活控制。这项技术揭示了遗传密码可被重新定义的性质,显著提升了科研人员设计和合成带有复杂非天然氨基酸修饰蛋白质的能力。
我院博士生方誉、博士后于微是论文的共同第一作者,林世贤研究员和医学院附属第四医院的丁文龙研究员是本文的通讯作者。研究工作得到了何向伟教授的大力帮助。该研究主要受国家自然科学基金项目的支持。
原文链接:https://www.nature.com/articles/s41557-026-02084-y
林世贤实验室聚焦于中心法则的翻译过程,整合交叉学科的研究手段,探索tRNA和蛋白质修饰的生物学功能和工程改造,并致力于开发新型生物医药,用于重大代谢慢病和罕见遗传病的诊疗。团队近五年在Science、Nat. Cell Biol.、Nat. Chem. Biol.、Nat. Chem.、Nat. Struct. Mol. Biol.等期刊发表研究成果。欢迎感兴趣的博士后和研究生联系并申请加入。
实验室链接:https://person.zju.edu.cn/0017079