2026年5月5日,我院蒋超研究员与何向伟教授合作在国际期刊《美国国家科学院院刊》(PNAS)在线发表了题为“Microhomology-mediated tandem duplication is a conserved mechanism of genomic variation with implications for human disease”的研究论文。该研究首次系统性地证明,微同源介导的串联重复(Microhomology-mediated Tandem Duplication, MTD)是一种在细菌、古菌、真菌乃至病毒中普遍存在的基因组变异机制,并揭示了其与人类疾病(包括癌症、代谢性疾病及神经系统疾病)的密切关联。

基因组上的串联重复序列(Tandem repeats,即相同或相似的DNA序列首尾相连排列)具有高度不稳定性,其拷贝数变化与亨廷顿舞蹈症、多种癌症及代谢性疾病的发生发展密切相关。然而,这些串联重复序列最初是如何起源的,长期以来是进化生物学和医学遗传学领域的一个未解之谜。早在二十年前,研究人员基于酿酒酵母中串联重复的序列特征提出假说:单拷贝DNA片段若两侧存在短的同源序列(即“微同源臂”),可能通过某种机制发生串联重复,从而成为多拷贝重复序列的“原始种子”。实验室前期在裂殖酵母中首次发现了全基因组范围内普遍发生的MTD现象(Dan et al., 2021),但这一机制是否在更广泛的生物界中保守存在,以及它在人类疾病中的作用,此前尚缺乏系统性的证据。
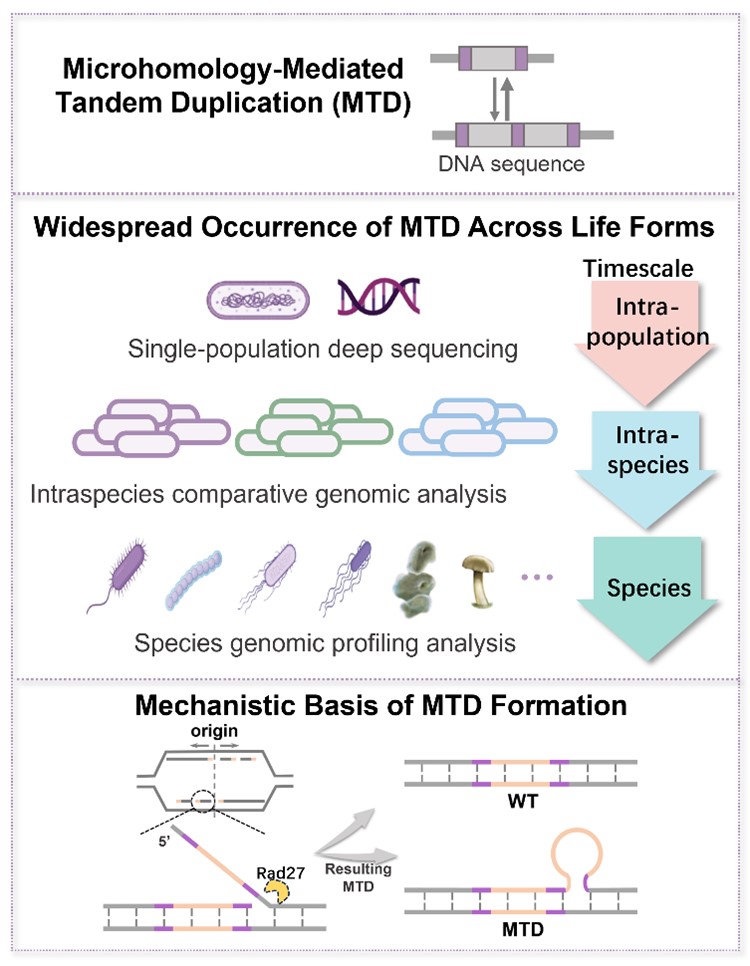
图1. MTD模型、生命域中保守和发生机制示意图。上:MTD模型图,表示在DNA序列上发生了一个单元的串联复制插入突变。紫色表示微同源臂,与一个重复核心区域(灰色)组成一个重复单元;中:探究MTD 在不同生命形式中的演化层面(种群内、物种内、物种)的普遍发生现象;下:MTD形成机制,在DNA复制过程中冈崎片段加工缺陷促成 MTD 的发生。
针对这一科学问题,本研究开发了一套统一的分析流程,结合全基因组深度测序与大规模公共数据库挖掘,对来自细菌、古菌、真菌、病毒以及人类的超过2200个参考基因组和数百万个分离株基因组进行了全面分析。结果发现,MTD事件在原核、真核及病毒基因组中普遍存在,在种群内、物种内及物种这三个演化尺度上均显著发生;考虑长期进化中的序列退化后,约80%的串联重复可归因于MTD机制,揭示了其跨生命形式与演化尺度的高度保守性。这一发现将MTD从原先仅在裂殖酵母中观察到的现象,拓展为整个生命界保守的基因组多样性产生机制。
本研究进一步揭示了MTD的进化动力学特征:绝大多数MTD事件在中性或近乎中性的选择压力下演化,但纯化选择会优先从编码区清除可能有害的MTD,从而保护基因功能。在机制层面,本研究通过在酿酒酵母中敲除保守的flap内切酶Rad27(哺乳动物FEN1的同源基因),发现MTD的从头形成频率显著升高,提示MTD的发生与冈崎片段成熟过程中的DNA复制修复相关。这一发现将DNA复制后加工与串联重复的起源直接联系了起来。
尤为重要的是,本研究在人类基因组中发现了大量微同源臂介导的串联重复事件。这些重复不仅存在于正常人群的多态性位点,也在疾病相关数据库中显著富集。特别是与基因组稳定性、癌症及代谢性疾病相关的致病性变异中,MTD特征尤为突出。这意味着MTD机制可能是人类疾病中一类尚未被充分认识的基因组变异来源。其遗传可逆特征为肿瘤发生、遗传病诊断以及潜在的治疗干预提供了新的切入点。
浙江大学生命科学研究院韦宪方博士为论文第一作者,蒋超研究员与何向伟教授为共同通讯作者。何向伟实验室博士生龚婉馨及张静博士;蒋超实验室博士生郑一帆和彭晨也参与了该项研究。该工作获得了国家自然科学基金委面上项目、国家科技重大专项、浙江省自然科学基金以及中央高校基本科研业务费的资助。
实验室主页:
http://lsi.zju.edu.cn/jianglab_exposome/list.htm
http://lsi.zju.edu.cn/25414/list.htm
原文链接:
https://www.pnas.org/doi/10.1073/pnas.2606747123