2021年6月14日,生命科学研究院任艾明课题组与奥地利因斯布鲁克大学Ronald Micura课题组合作在Nucleic Acids Research杂志上发表题为“Insights into xanthine riboswitch structure and metal ion-mediated ligand recognition”的研究论文,报道了特异性结合黄嘌呤的天然核开关NMT1 motif的晶体结构,揭示了由金属离子介导的黄嘌呤核开关对配体识别的原理。
核开关(Riboswitch)是一类位于mRNA 5’端非编码区域的不依赖于蛋白可直接调控基因表达的RNA元件,可以形成特定的三维空间结构。这类RNA元件含有两个不同功能的结构域,适配体模块(aptamer domain)可以特异性地识别小分子配体,并发生构象改变,从而诱导位于下游的基因表达调控模块(expression platform)的构象也随之发生改变,进而在转录或翻译水平上促进或者抑制相关蛋白的表达。目前已经发现和报道的核开关有四十余种,其可识别的小分子涵盖氨基酸,阴离子,金属离子,辅酶因子及其衍生物,嘌呤核苷酸及其衍生物等。
嘌呤及其衍生物是细胞内最为丰富的一类代谢物,广泛地存在于生命体中并发挥重要的生理作用,也因此嘌呤的代谢在细胞内受到严格的调控,代谢失调会导致严重的细胞紊乱。黄嘌呤(图A)是嘌呤降解代谢过程中的氧化产物,可在黄嘌呤氧化酶的作用下进一步氧化产生尿酸,广泛存在于人体及其他生物体内。2020年,耶鲁大学的Ronald Breaker课题组在变形杆菌中鉴定出一类新型RNA 结构模块(motif)NMT1,随后发现NMT1能够以微摩尔级别亲和力与黄嘌呤结合,因此将其称为黄嘌呤核开关。二级结构研究表明黄嘌呤核开关主要含有两个茎区P1和P2,它们由一个大的Junction(J1)连接;其中茎区P2又被中间含有的一个小Junction(J2)分为P2a,P2b两个小茎区。进一步分析显示,黄嘌呤核开关中位于连接处的核苷酸序列高度保守(图B)。
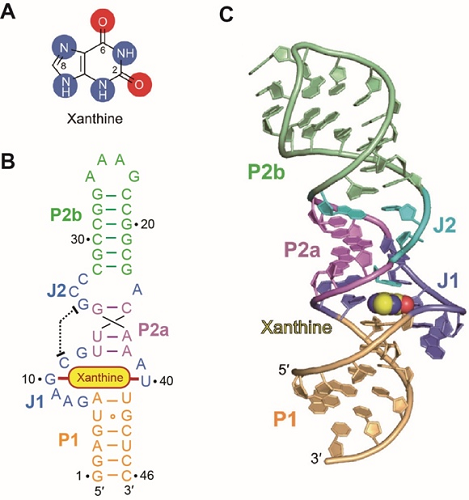
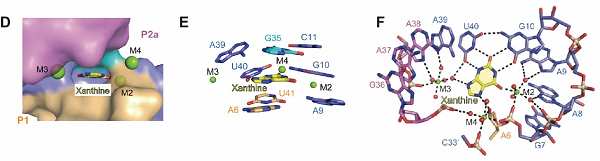
为了阐明黄嘌呤核开关识别其配体的原理以及其对嘌呤代谢通路的调控作用,任艾明课题组利用X-射线晶体学的方法,解析了来自Ideonella sp. B508-1中的黄嘌呤核开关与黄嘌呤的复合物结构(图C)。复合物的三维结构显示,黄嘌呤核开关RNA整体折叠为一个紧凑的长杆状I形构象,茎区P1,P2a,P2b在三维空间中连续堆积形成长的螺旋轴。两个Junction(J1,J2)通过G35和C11之间的Watson-Crick配对形成远程相互作用,稳定了黄嘌呤核开关的整体结构。配体结合口袋处于茎区P1和P2a之间的连接区,其中黄嘌呤与G10和U40作用形成一个三碱基层,该三碱基层被进一步夹在两个三碱基对A39-G35-C11和A6-U41-A9之间,成为长螺旋轴的重要组成部分(图D, E)。此外,结构中还发现,黄嘌呤结合位点附近存在三个金属离子Mg2+(M2,M3,M4),它们通过直接作用或者配位水分子的介导,与配体黄嘌呤以及形成结合口袋的核苷酸形成广泛的氢键相互作用,进而稳定结合口袋的形成(图F)。基于结构,我们对结合口袋中的关键碱基进行了特异性突变,随后通过ITC亲和力测定以及2-Ap修饰RNA 分子的荧光光谱分析,进一步验证了黄嘌呤核开关对黄嘌呤特异性识别的结构特征。
本项研究通过解析黄嘌呤核开关的三维空间结构以及相关的生物化学和动力学研究,揭示了黄嘌呤核开关对配体高特异性识别的分子基础,阐明了细菌通过RNA分子调控嘌呤代谢的作用机制。同时,新的RNA结构也进一步丰富了RNA分子的结构数据库。黄嘌呤作为一种重要的生物碱和嘌呤代谢的中间产物,可衍生出多种黄嘌呤类药物,这些与痛风等疾病息息相关,关于黄嘌呤核开关RNA的高级结构的研究为发展抗生素、生物传感器等提供必要的结构基础。
该研究工作获得了国家自然科学基金(32022039, 31870810, 91940302, 91640104, 31670826),浙江省杰出青年基金(LR19C050003)以及浙江大学中央高校基金科研项目业务费(2017QN81010)等项目的资助。浙江大学生命科学研究院博士生许笑晨和陈豪同学为本文的共同第一作者。
原文链接:https://doi.org/10.1093/nar/gkab486