2022年2月23日,我院祝赛勇实验室在Science Advances发表题为“Human expandable pancreatic progenitor-derived β cells ameliorate diabetes”的研究论文。该研究发现含溴结构域和额外终端域家族蛋白抑制剂I-BET151可以有效促进人胰岛前体细胞(Pancreatic progenitors, PPs)的扩增,并通过进一步优化,成功建立了人胰岛前体细胞高效扩增培养新体系。
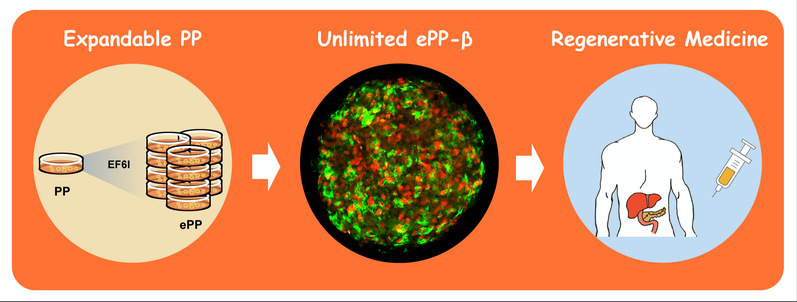
图1. 人胰岛前体细胞高效扩增培养新体系及其临床转化
糖尿病是一种全球高发慢性病,严重影响着数亿人健康。胰岛移植是糖尿病治疗中极具前景的一种方法,但该疗法仍面临供体来源短缺、免疫排斥等限制因素。人多能干细胞分化为胰岛细胞技术为治疗这一疾病带来希望。
本研究中,祝赛勇实验室首先将人多能干细胞分化为胰岛前体细胞。随后,团队进行小分子文库筛选,并幸运地发现了I-BET151可以显著提高PDX1和NKX6.1双阳性胰岛前体细胞的比例。通过反复验证和优化,最终建立了可扩增的胰岛前体细胞(expandable PPs, ePPs)的培养体系。利用该条件,胰岛前体细胞可以稳定冻存和复苏,并且实现了长期稳定培养扩增。在培养过程中,这些可扩增的胰岛前体细胞维持了前体细胞的特征、稳定的核型和自我更新能力。特别重要的是,这些胰岛前体细胞系可以进一步高效分化为功能成熟的胰岛β细胞(ePP-β)及胰岛类器官,将ePP-β细胞移植到小鼠体内后能够存活并维持胰岛细胞特征,而且小鼠的糖尿病得到了显著改善。在机制方面,I-BET151可以特异性促进胰岛前体细胞标志基因位点的染色质可及性,加强其增强子水平,从而上调关键标志基因的表达,并稳定胰岛前体细胞的基因调控网络。
综上所述,该研究首次建立了人胰岛前体细胞长期稳定高效扩增的培养体系,通过扩增培养获得的人胰岛前体细胞能够进一步快速高效地分化为具有生理功能的人胰岛细胞,实质性优化了大量制备具有生理功能的人胰岛细胞及胰岛类器官的技术难题,因而在细胞疗法、疾病模型、药物筛选和基础研究等方面具有广泛的应用前景。
祝赛勇实验室博士后马晓洁为论文第一作者,祝赛勇研究员为本论文通讯作者。该研究受到了国家自然科学基金、科技部重点研发计划、浙江省杰出青年基金、中国博士后科学基金等项目的资助。实验室常年招收具有分子细胞生物学研究背景的研究生与博士后,欢迎访问网站了解详细信息(http://lsi.zju.edu.cn/25630/list.htm)。