器官发育是最重要的生物学问题之一。通过研究线虫、果蝇、斑马鱼、爪蟾、小鼠等经典模式生物,建立了发育学基本原理。人多能干细胞定向分化及类器官技术,基于人类自身遗传背景,是研究人类器官发育新体系,具有独特性、不可替代性。近年来,这一领域得到了快速发展,越来越受到重视、关注和应用。特别是利用干细胞定向分化结合CRISPR基因编辑技术,研究细胞分化和器官发育,已成为研究热点。其中胰岛类器官技术,不仅可以促进胰腺发育生物学研究,而且在糖尿病治疗方面极具临床转化前景。
细胞分化和器官发育依赖于复杂的调控网络,包含转录因子、表观调控因子、信号通路等。N6-甲基腺嘌呤(m6A)是哺乳动物mRNA内部丰度最高的化学修饰,是当前最受关注的表观转录组修饰。m6A修饰在METTL3、METTL14、WTAP以及其他辅助蛋白组成的甲基转移酶复合物的作用下形成,该甲基化修饰可被去甲基化酶ALKBH5和FTO去除。m6A识别蛋白,包括YTHDF1-3、YTHDC1-2、IGF2BP1-3等,可以特异性结合mRNA m6A,调控mRNA代谢,包括加工、输出、稳定性、翻译等。目前,m6A修饰及其关键因子在人胰腺分化和发育中的动态调控与作用机制还未见报道。
2022年7月18日,生研院祝赛勇、高分子系刘建钊课题组合作在Nature Communications发表题为“N6-methyladenosine modification-mediated mRNA metabolism is essential for human pancreatic lineage specification and islet organogenesis”的研究论文,首次绘制了整个人胰腺分化过程中的mRNA m6A修饰的动态变化图谱,详细研究了m6A修饰对于胰腺细胞分化过程的基因表达调控,并揭示去甲基化酶ALKBH5在胰腺谱系分化和胰岛类器官发育过程中起着关键作用。
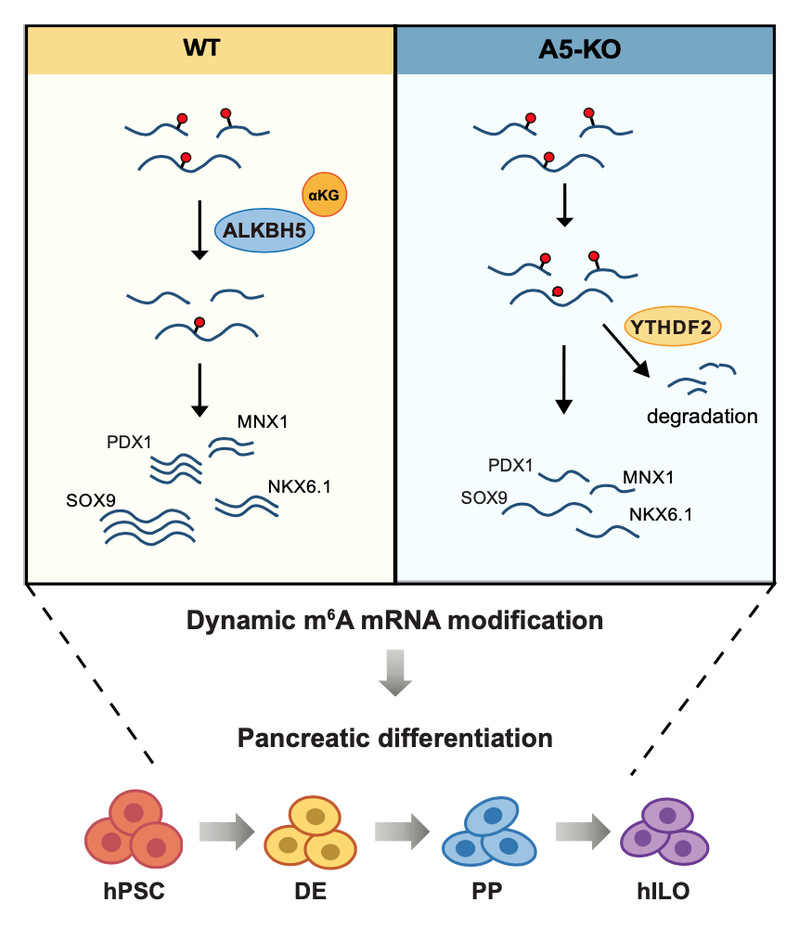
图1. 胰腺分化过程中mRNA m6A修饰动态及ALKBH5的关键调控作用
本研究基于最新的人多能干细胞向胰岛类器官分化体系,在人多能干细胞(hPSC)、定型内胚层细胞(DE)、胰岛前体细胞(PP)、人胰岛类器官(hILO)阶段收集样品,进行m6A-seq和RNA-seq分析,结果显示在胰腺分化过程中,mRNA m6A修饰呈现出阶段特异性和多样性。随后,研究团队发现ALKBH5敲除显著抑制多能干细胞向胰岛前体细胞分化,并影响胰岛类器官生成。分子机制方面,ALKBH5敲除会增加胰腺分化过程中关键转录因子(PDX1、 NKX6.1、SOX9和MNX1)的m6A修饰水平,并被m6A识别蛋白YTHDF2识别,进而介导这些mRNA的降解,导致胰岛前体细胞分化受到抑制。重要的是,研究团队发现ALKBH5的辅助因子ɑKG可以提高人多能干细胞向胰岛前体细胞分化效率,并进一步促进胰岛细胞高效制备。
综上所述,该研究详细绘制了人多能干细胞向胰岛类器官分化过程中mRNA m6A动态变化图谱,揭示了其阶段特异性和多样性;通过构建ALKBH5敲除人多能干细胞系,深入研究了ALKBH5在胰腺分化过程中的重要功能;该工作提示可以通过ɑKG-ALKBH5-m6A-YTHDF2途径,从RNA甲基化修饰层面,精准调控细胞分化和器官发育。
浙江大学祝赛勇研究员和刘建钊教授为论文的共同通讯作者,博士后马晓洁、博士后曹婕、博士生周恣羽、博士生陆云昆为论文的共同第一作者。该研究受到了国家自然科学基金、科技部重点研发计划、浙江省杰出青年基金、中国博士后科学基金等项目的资助。