卵母细胞是哺乳动物体内最大的细胞,但其如何生长成为最大的细胞,还没有具体的科学解释。卵巢中储存的原始卵泡激活以后,卵泡中的卵母细胞要经历为期数周的生长期,体积明显增大,并且在卵胞质中积累了大量转录加工成熟的mRNA。这些mRNA与体细胞中的mRNA相比,有以下几个特点:1)体细胞中的mRNA很不稳定,半衰期只有3分钟左右;而卵母细胞中的mRNA非常稳定,半衰期达到12天以上。2)体细胞中的mRNA在细胞核中已经加上了较长的poly(A)尾(约150 - 250 bp),运送到细胞质中以后马上被翻译成蛋白质;而卵胞质中的大多数mRNA poly(A)尾较短(约30 – 80 bp),蛋白翻译活动并不活跃。3)体细胞中的mRNA poly(A)尾被多种去腺苷酸化酶切短以后就会发生不可逆的降解;但卵胞质中的mRNA在减数分裂成熟、受精、早期胚胎发育的多个阶段,发生可逆的poly(A)尾缩短和再延长,从而实现发育时期特异性的mRNA翻译调控(Sha et al., 2019)。虽然已知mRNA 3ʹ-UTR中的顺式作用元件与多种RNA结合蛋白的复杂协同机制在卵子成熟过程中调控着poly(A)尾的延长和缩短(Dai et al., 2018),但伴随着卵子生长过程而发生的mRNA转录后加工调控,目前还所知甚少。
近日,生研院范衡宇团队在Science Advances发表题为“PABPN1 Functions as a Hub in the Assembly of Nuclear Poly(A) Domains that are Essential for Mouse Oocyte Development”的研究论文,首次报道小鼠卵母细胞中的新生mRNA定位在细胞核的一个特定功能区域,并命名为nuclear poly(A) domain (NPAD)中。Poly(A)结合蛋白PABPN1通过液-液相分离机制调控卵子发生过程中mRNA的转录后加工。
研究团队首先利用荧光分子原位杂交技术,检测到带有poly(A)的mRNA聚集在生长期卵母细胞中的细胞核特定区域,即nuclear poly(A) domain(NAPD)中。该亚细胞结构具有如下特征:1)只特异性地存在于卵母细胞中,而在体细胞中检测不到,这可能与卵母细胞中独特的mRNA加工和存储模式密切相关;2)动态存在于次级卵泡和早期有腔卵泡的卵母细胞中,而在转录终止的排卵前卵母细胞中消失(图1A-B);3)其存在依赖于卵母细胞核中的转录活性;4)与细胞核中的poly(A)结合蛋白PABPN1、剪切因子SRSF2(也称SC35)和CPSF4等RNA结合蛋白共定位(图1C)。
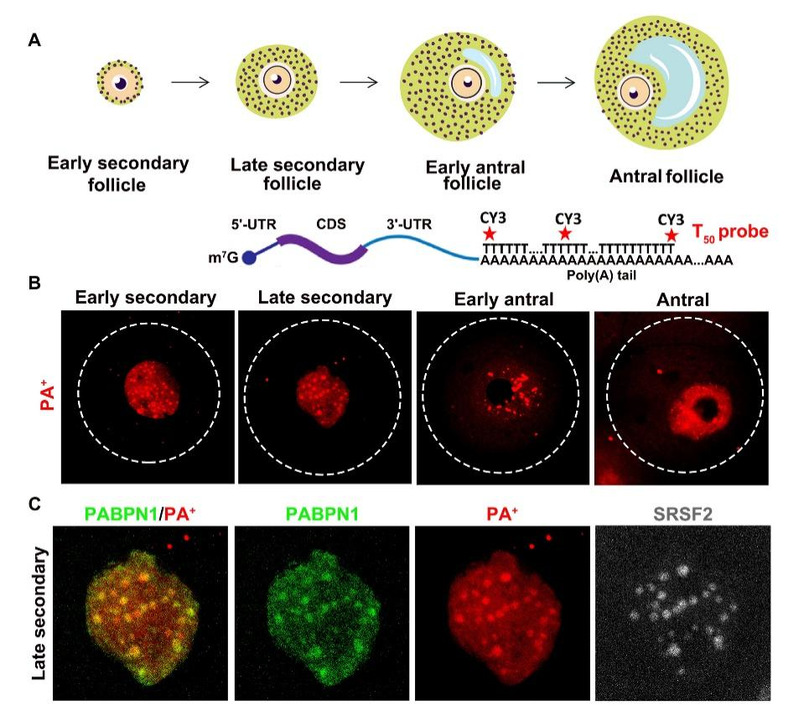
图1:卵母细胞中的nuclear poly(A) domain(NPAD)。
A: 卵泡发育过程及poly(A)原位杂交探针设计。B: Poly(A) RNA在卵母细胞中的定位。C:PABPN1和SRSF2(SC35)的共定位。
进而,研究团队发现PABPN1对于nuclear poly(A) domain结构的形成和维持至关重要,因为在卵母细胞中特异性敲除Pabpn1基因会阻止NAPD结构的形成(图2A),而过表达PABPN1的卵母细胞中则形成更大的nuclear poly(A) domain。生化机制研究表明,PABPN1一方面通过其N端的内在无序结构域(intrinsically disordered region,IDR)而相互聚集成液态胶体状,与周围环境形成液-液相分离,另一方面通过其C端的RNA结合结构域把具有poly(A)尾的mRNA聚集到以PABPN1为主体的蛋白质微胶体球中,而polyA mRNA进一步促进了PABPN1微胶体的形成。另外,PABPN1也通过募集多种RNA结合蛋白,在nuclear poly(A) domain形成一个复杂、高效的mRNA剪切和加尾微环境。
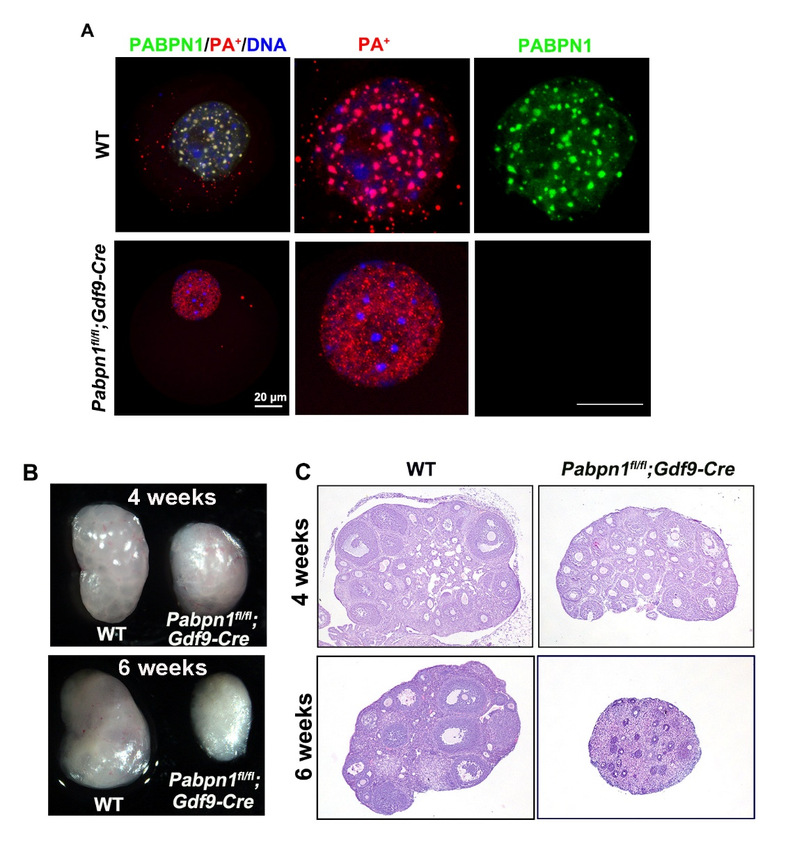
图2:PABPN1在卵母细胞中的生理功能。
A:Pabpn1敲除影响NPAD的正常形成。B-C:卵母细胞特异性Pabpn1敲除导致卵泡发育异常和卵巢早衰。
卵母细胞特异性敲除Pabpn1的小鼠表现为卵泡发育受阻、卵巢早衰、不能排卵、雌性完全不育(图2B-C)。在分子水平上,卵母细胞中不能有效建立起母源mRNA储备,生成的mRNA由于poly(A)尾长度短于正常范围而不稳定,半衰期变短,翻译能力降低;而且由于不能向nuclear poly(A) domain中有效募集CPSF蛋白,使mRNA的3ʹ-UTR剪切存在异常,改变了转录组中各种剪切异构体之间的正常比例。这些体内研究结果,证明以PABPN1相变为核心的nuclear poly(A) domain,具有富集RNA结合蛋白,对新生RNA进行剪切、加尾、保护和储存的重要功能,并且对于决定卵母细胞的发育潜能具有重要生理意义。
课题组在先前的研究中,曾经报道了一个在脊椎动物卵母细胞和早期胚胎中特异性表达的PABPN家族成员,PABPN1L,在母源-合子过渡(maternal-to-zygotic transition,MZT)过程中与MZT准入因子BTG4协同作用,介导母源mRNA的及时降解(Zhao et al., 2020)。在另一篇研究论文中发现,PABPN1与PABPN1L在小鼠卵子发生和母源-合子过渡过程中具有时间窗口互补的表达模式,早期胚胎发育过程中表达的PABPN1,通过招募特异性降解尿苷化修饰的3ʹ-5ʹ核酸外切酶DIS3L2,到TUT4/7调节的3ʹ-端尿苷化修饰的母源mRNA上,促进胚胎期母源mRNA降解(zygotic mRNA decay, Z-decay)的顺利进行(Zhao et al., 2022)。而本研究的结果显示,PABPN1L并不定位在nuclear poly(A) domain;在缺失PABPN1的卵母细胞中回补PABPN1L也不能恢复nuclear poly(A) domain的结构和功能,说明对nuclear poly(A) domain是PABPN1独有的生化功能,这是因为PABPN1L蛋白结构中不具有发生相变所需的内在无序区域IDR。
范衡宇团队通过这些系列研究,发现PABPN家族的两种poly(A)结合蛋白在卵母细胞和早期胚胎中具有时空特异性功能,密切调控母源mRNA的剪切、定位、储存、加尾、翻译和降解。而细胞核和细胞质中丰富的mRNA积累和有序储存,以及空间的区域化和RNA结合蛋白的相变过程,为卵母细胞成长为体内最大的细胞提供了重要的生化基础(图3)(Zhao and Fan, 2021)。本研究的匿名评审专家也在评审意见中指出:“在本文中作者研究了PABPN1在生长卵母细胞中调控新生mRNA的功能,命名了新的细胞核亚细胞结构域NPAD,并解析了与NPAD相变相关的PABPN1结构域及其他互作蛋白。更进一步地,作者通过建立Pabpn1条件性敲除小鼠品系,证明缺失该基因的雌鼠卵子发生失败并完全不育。这些结果有趣并重要,因为我们对于卵子发生过程中mRNA如何被加工和储存的知识还非常缺乏。”
范衡宇团队博士后戴兴兴、博士生皮帅玻、博士生赵龙雯(已毕业)为本文共同第一作者。该研究受到了国家重点研发计划、国家自然科学基金、浙江省自然科学基金、中国博士后科学基金等项目的资助。
原文链接:https://www.science.org/doi/10.1126/sciadv.abn9016
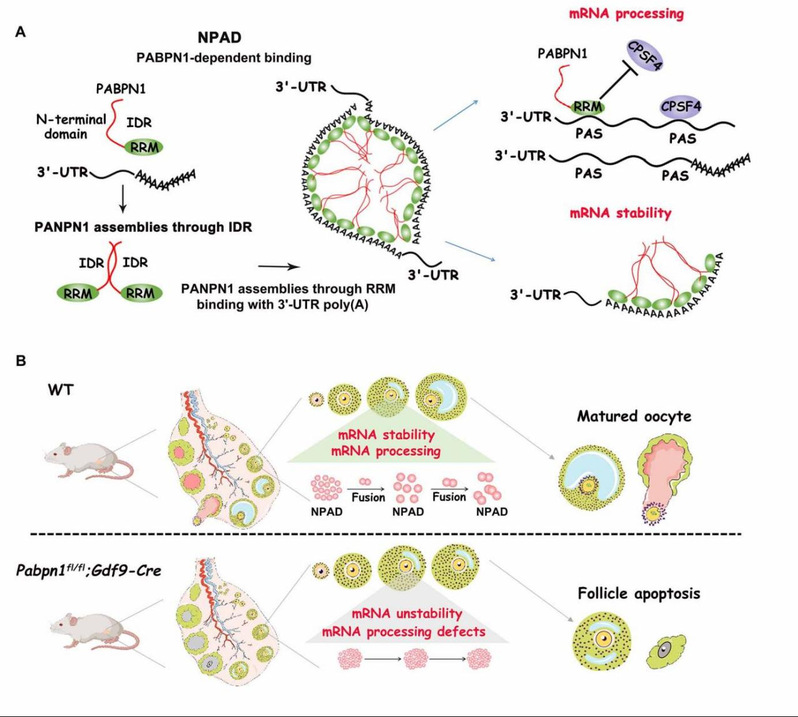
图3:PABPN1相分离机制的生化和生理功能总结。
参考文献
Dai, X.X., Jiang, J.C., Sha, Q.Q., Jiang, Y., Ou, X.H., Fan, H.Y., 2018. A combinatorial code for mRNA 3'-UTR-mediated translational control in the mouse oocyte. Nucleic Acids Res.
Sha, Q.Q., Zhang, J., Fan, H.Y., 2019. A story of birth and death: mRNA translation and clearance at the onset of maternal-to-zygotic transition in mammalsdagger. Biol Reprod 101, 579-590.
Zhao, L.W., Fan, H.Y., 2021. Revisiting poly(A)-binding proteins: Multifaceted regulators during gametogenesis and early embryogenesis. Bioessays, e2000335.
Zhao, L.W., Zhu, Y.Z., Chen, H., Wu, Y.W., Pi, S.B., Chen, L., Shen, L., Fan, H.Y., 2020. PABPN1L mediates cytoplasmic mRNA decay as a placeholder during the maternal-to-zygotic transition. EMBO Rep, e49956.
Zhao, L.W., Zhu, Y.Z., Wu, Y.W., Pi, S.B., Shen, L., Fan, H.Y., 2022. Nuclear poly(A) binding protein 1 (PABPN1) mediates zygotic genome activation-dependent maternal mRNA clearance during mouse early embryonic development. Nucleic Acids Res 50, 458-472.