2024年1月22日,《Nature Cell Biology》期刊以研究长文的形式发表了生研院徐平龙实验室、浙大转化院沈承勇实验室、浙大科创中心李欣然博士的合作研究论文,题为“Innate immune sensing of lysosomal dysfunction drives multiple lysosomal storage disorders”。该工作以遗传学、病理学、生化以及细胞生物学技术首次明确鉴定了神经元中存在显著激活的cGAS-STING天然免疫机制及其驱动体内神经元死亡和神经疾病发生的关键功能。研究聚焦其在识别和应答溶酶体损伤中的核心功能,阐明其驱动多种溶酶体贮积症发病,并提出了一种通用的治疗溶酶体贮积症的新策略。
cGAS-STING信号通路是进化上高度保守的、广泛分布于几乎所有类型细胞的组织损伤识别机制。该通路以经典或非经典的信号转导路径调控多种细胞生理过程,包括细胞自噬、蛋白质合成、DNA损伤修复、糖脂代谢、无膜细胞器组装、细胞衰老等。溶酶体贮积症(Lysosomal storage disorders, LSDs) 是一类以溶酶体功能障碍和代谢异常为特征的遗传性疾病。溶酶体功能障碍导致功能性细胞的进行性死亡是引发退行性疾病的关键因素,也是60多种溶酶体贮积症的直接病因,严重威胁人类生命健康。然而,溶酶体功能障碍诱导功能性细胞进行性死亡的具体分子机制目前仍不清楚,同时尚且缺乏通用性的治疗贮积症的药物或其他干预手段。徐平龙实验室的早期研究中发现多种神经元存在活跃的cGAS-STING天然免疫机制。在由HEXB、GLA、CTSD、NPC1和GBA等基因异常驱动的多种溶酶体贮积的神经元等细胞模型中,他们意外发现cGAS-STING信号通路能够显著并持续性激活。深入研究其分子机制,他们发现贮积症模型小鼠的神经元胞质中积累了大量双链DNA(dsDNA),并伴随着DNA感受器cGAS的出核以及高水平的第二信使cGAMP的产生,从而显著激活STING通路。遗传和体外模型则证明神经元STING通路导致神经元的大规模丢失。值得注意的是,多种干预神经元cGAS-STING通路的策略,如全身性或神经细胞谱系特异性的基因敲除cGAS或STING,能显著抑制贮积症模型小鼠中神经元的死亡和神经炎症的发生,有效改善小鼠的运动功能障碍。此外,实验室利用AAV载体在贮积症模型动物的中枢神经系统中引入细胞质定位的DNA外切酶,以清除神经元胞质中的双链DNA(dsDNA)。这一创新的基因治疗手段能显著缓解多种LSD小鼠的疾病表型。
这些重要发现明确鉴定了神经元中存在显著的cGAS-STING天然免疫机制,发现了cGAS-STING通路感知溶酶体功能障碍的新功能,揭示了神经元cGAS-STING通路在体内神经元生死命运决定中的关键作用。这些工作建立了溶酶体缺陷与天然免疫之间的关键联系,并提出了由cGAS-STING信号通路介导的损伤识别机制是多种溶酶体贮积症发病的共性机制。这项研究在转化研究领域有重要创新,为溶酶体贮积症的治疗提供了一种通用的新策略。
徐平龙实验室博士后王爱莲、博士生陈琛为论文共同第一作者,徐平龙教授、沈承勇教授和李欣然研究员为通讯作者, 实验室梅陈博士和刘盛铎博士等同学也有重要贡献。研究工作也得到了冯新华教授、梁庭波教授、邹键教授、叶存奇研究员、夏冰教授、Dante Neculai教授、林爱福教授、白雪莉教授、章琦教授和陈莎莎教授等合作者的大力支持。该项研究受到基金委重点项目、杰青项目和科技部重点研发计划等项目资助,在浙江大学开展并完成。
附徐平龙实验室研究员、博士后招聘
徐平龙实验室运用跨学科研究技术体系,长期从事天然免疫识别的信号机制、调控及生理病理功能研究,在核酸免疫识别的细胞和病理功能及新型信号机制等方向有系统性贡献,研究工作发表于Nature Cell Biology (2024, 2022, 2019, 2017)、Molecular Cell (2022, 2021, 2020, 2014)、Cell Host & Microbe (2017) 等知名学术期刊,获基金委创新群体、国家杰青、重点项目、科技部重点研发等多项基金资助。因研究拓展需要,长期公开聘用分子细胞、神经、病理、代谢、感染免疫、细胞工程、生物材料、病毒、生物信息、药学等领域研究员或者博士后3-4名。岗位要求:对科学探索有浓厚兴趣和创新思维,有较强的独立科研工作能力和英文写作能力,富有团队合作精神。实验室提供优良的工作环境、科研平台和竞争性薪酬。有意向者请将个人简历和1-2篇已发表的代表作发送至xupl@zju.edu.cn。
原文链接:https://www.nature.com/articles/s41556-023-01339-x
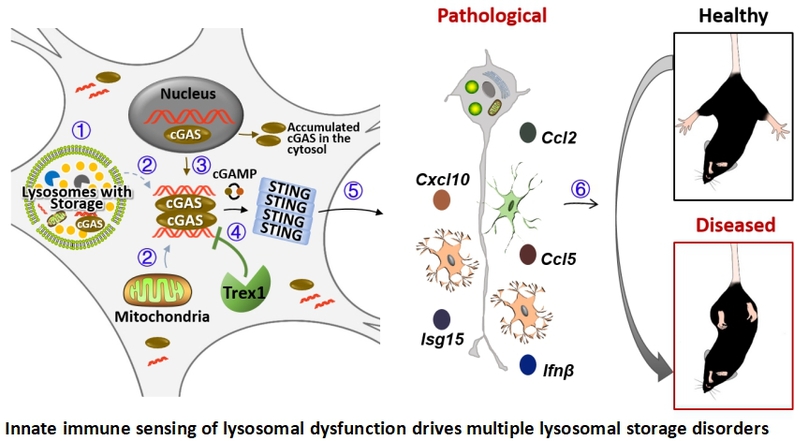
溶酶体功能障碍的先天免疫感知驱动多种溶酶体贮积症